Un médicament de transplantation utilisé depuis des décennies peut préserver la fonction des cellules productrices d’insuline chez les jeunes enfants nouvellement diagnostiqués avec le diabète de type 1.

Les personnes atteintes de diabète de type 1 doivent s’injecter de l’insuline pour survivre. Mais un nouvel essai suggère qu’un médicament de transplantation peu coûteux pourrait retarder la progression de la maladie.(Crédit image : Javier Zayas Photography/Getty Images)Abonnez-vous à notre newsletter
Un médicament abordable utilisé depuis des décennies dans les chirurgies de transplantation peut retarder la progression du diabète de type 1 chez les nouveaux diagnostiqués, suggèrent de nouvelles recherches.
Dans des études antérieures, une forte dose du médicament immunosuppresseur globuline antithymocyte polyclonal (ATG) a réduit la perte des cellules productrices d’insuline dans le pancréas, appelées cellules bêta. La nouvelle étude montre qu’une dose beaucoup plus faible est presque aussi efficace pour ralentir la progression de la maladie de type 1, mais avec moins d’effets secondaires.
Cependant, il existe une période peu après le diagnostic, appelée “phase lune de miel”, pendant laquelle les cellules bêta produisent encore de l’insuline ; cela offre une opportunité de maintenir ces cellules bêta restantes en vie plus longtemps. Une phase lune de miel plus longue et une fonction résiduelle des cellules bêta plus importante sont liées à un risque réduit de complications du diabète, telles que les maladies cardiaques et rénales, à long terme.
C’est cette phase lune de miel que la nouvelle étude visait. L’étude comprenait 117 participants, âgés de 5 à 25 ans et diagnostiqués avec le diabète de type 1 dans les neuf semaines suivant le début de l’essai. Les participants ont reçu soit une forte, une intermédiaire, soit une faible dose d’ATG : la forte dose était équivalente à 2,5 milligrammes d’ATG par kilogramme de poids corporel ; la dose intermédiaire était de 1,5 mg/kg ; et la faible dose était de 0,5 mg/kg de poids corporel.
Les chercheurs ont constaté que la dose la plus faible préservait la fonction des cellules bêta pendant un an, selon l’article publié le 27 septembre dans la revue The Lancet.
L’essai a été conçu pour aider les chercheurs à analyser la dose efficace la plus faible chez les enfants dès l’âge de 5 ans, a déclaré à Live Science la Dre Chantal Mathieu, endocrinologue à l’Hôpital Universitaire Gasthuisberg Leuven en Belgique, auteure principale de l’étude. En effet, les effets secondaires du médicament, tels que des réactions immunitaires nocives, peuvent être particulièrement difficiles pour eux, a-t-elle ajouté.
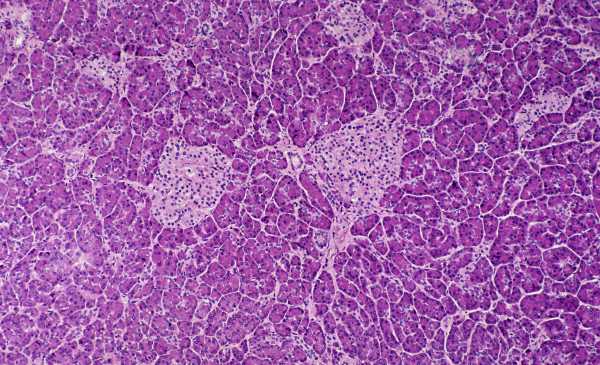
Dans le diabète de type 1, le système immunitaire détruit les cellules bêta situées dans les îlots de Langerhans du pancréas (montrés ici). (Crédit image : Ed Reschke/Getty Images)
“L’ATG a fonctionné merveilleusement bien”, a-t-elle dit. L’effet bénéfique “était le plus important chez les plus jeunes enfants”.
C’était la troisième étude à confirmer l’efficacité de l’ATG pour retarder la perte des cellules bêta, a ajouté Mathieu.
Notamment, lorsque les chercheurs ont examiné les données, ils ont constaté un niveau similaire d’effets secondaires dans les groupes à dose intermédiaire et forte, ils ont donc abandonné la dose intermédiaire des études futures. La principale différence entre les groupes à forte et à faible dose restants était l’incidence des effets secondaires. L’un des effets secondaires les plus courants de l’ATG est le syndrome sérique, une réaction immunitaire aux protéines étrangères qui peut être déclenchée par des médicaments fabriqués dans les cellules d’autres animaux. (L’ATG est produit dans les cellules de lapins et de chevaux.) Dans la nouvelle étude, le syndrome sérique a touché 82 % des participants du groupe à forte dose et seulement 32 % dans le groupe à faible dose.
Pendant ce temps, dans le groupe à faible dose, 24 % ont présenté un syndrome de libération de cytokines, une réponse inflammatoire incontrôlable qui peut inclure de la fièvre, des nausées, de la fatigue, des maux de tête et des douleurs musculaires et articulaires. Environ 33 % des participants ayant reçu la dose plus élevée ont développé le syndrome.
“Je pense que la raison pour laquelle c’est quelque peu prometteur, c’est qu’il s’agit maintenant de l’un des quelques médicaments qui montrent qu’on peut quelque peu retarder le diabète de type 1”, a déclaré Mathieu. Un autre avantage de l’ATG, selon Mathieu, est qu’il est peu coûteux et largement disponible.
D’autres médicaments qui se sont avérés retarder le diabète sont le teplizumab-mzwv (nom de marque Tzield) et le baricitinib (Olumiant). Le Tzield est administré en perfusion de 14 jours, mais il n’est approuvé que pour une utilisation dans le diabète de “stade 2” – à ce stade, le corps produit des anticorps contre l’insuline et présente des réponses anormales de la glycémie, mais la plupart de ses cellules productrices d’insuline fonctionnent encore. Peu de personnes sont diagnostiquées à ce stade précoce, ce qui limite la portée du médicament.
Pendant ce temps, le baricitinib – un médicament contre la polyarthrite rhumatoïde qui n’a pas encore été testé chez les enfants diabétiques – doit être pris en continu pour prévenir la progression de la maladie.
Bonnes nouvelles pour les jeunes enfants
La Dre Jennifer Sherr, endocrinologue et professeure de pédiatrie à la Yale School of Medicine, qui n’a pas participé à l’étude, a déclaré que les résultats étaient encourageants, en particulier pour les familles qui auraient énormément de mal à s’absenter du travail pour que leur enfant reçoive deux jours de perfusions. Dans l’étude, les personnes du groupe à faible dose ont reçu une perfusion le premier jour et un placebo le second jour, mais le jour du placebo ne serait pas nécessaire si le médicament était administré en dehors d’un essai clinique, a-t-elle noté.
Sherr a également apprécié que l’étude inclue des enfants âgés de 5 à 11 ans. “Ce sont les enfants qui perdent leurs cellules bêta si rapidement” après le diagnostic, a dit Sherr à Live Science. “Leurs besoins en insuline augmentent incroyablement.”
Sherr espère que ce médicament moins coûteux pourrait finalement être approuvé pour une utilisation dans le diabète afin d'”aider les enfants à avoir une vie plus douce”, a-t-elle dit.
Quant à savoir si l’ATG est meilleur que d’autres alternatives démontrées pour retarder la progression, “beaucoup de gens pensent qu’il faudra une approche multimodale”, a-t-elle dit. En d’autres termes, pour vraiment arrêter le DT1 dans son élan, les gens auraient probablement besoin de plusieurs médicaments, a dit Sherr.
Il est prématuré de dire qu’un traitement est meilleur qu’un autre. “Je pense que ce qui nous donne espoir pour l’avenir, c’est qu’il y a beaucoup de choses que nous pouvons envisager”, a dit Sherr.
Et dans un essai clinique dont le début est prévu fin de cette année ou début de l’année prochaine, les chercheurs testeront une version de nouvelle génération d’ATG fabriquée dans des vaches génétiquement modifiées chez des personnes nouvellement diagnostiquées avec le diabète de type 1.
Le nouveau médicament, fabriqué par SAB BIO et appelé SAB-142, est cultivé dans une vache génétiquement modifiée pour produire des anticorps humains, a déclaré le chercheur principal, le Dr Michael Haller, chef de l’endocrinologie pédiatrique à l’Institut du diabète de l’Université de Floride et membre du conseil consultatif de SAB BIO. . “La vache peut ensuite donner son sang”, à partir duquel les anticorps humains sont récoltés, a dit Haller à Live Science par e-mail.
L’espoir est que, puisque les anticorps sont fabriqués à l’aide de gènes humains, ils ne déclencheront plus de syndrome sérique chez les patients. Les anticorps humains sont également moins susceptibles de provoquer la production d’anticorps par le système immunitaire qui bloquent l’action du médicament, donc en théorie, a dit Haller, “le nouveau médicament pourrait être plus sûr et même plus efficace dans le diabète de type 1.”
Note de l’éditeur : Haller détient des options d’achat d’actions dans SAB BIO, en plus d’être membre du conseil consultatif.
