Le malattie da prioni, come la “mucca pazza”, sono causate da proteine trasmissibili identificate negli anni ’80.
I prioni sono proteine mal ripiegate e non contengono materiale genetico, a differenza di batteri o funghi, tuttavia possono essere trasmessi tra organismi. (Crediti immagine: Love Employee via Getty Images) Iscriviti alla nostra newsletter
Il 9 aprile 1982, un medico dell’Università della California, San Francisco, pubblicò un articolo sulla rivista Science che dimostrava come proteine infettive causassero una malattia neurologica degenerativa nelle pecore. In questo modo, trasformò la nostra comprensione di come alcune malattie vengono trasmesse.
“In quel periodo, stavo iniziando una specializzazione in neurologia e rimasi molto colpito da un processo patologico che poteva uccidere il mio paziente in due mesi distruggendo il suo cervello, mentre il suo corpo rimaneva inalterato da questo processo”, disse in un discorso che tenne in seguito sulla sua scoperta.
Negli anni ’50, il termine “virus lento” era stato coniato per descrivere le malattie scrapie in pecore e capre. Negli anni ’60, gli scienziati avevano iniziato ad applicare il termine a certi disturbi umani, notando che la malattia “kuru” che aveva devastato la tribù Fore in Papua Nuova Guinea sembrava essere trasmessa quando i membri della tribù mangiavano i cervelli di coloro che erano morti in precedenza della malattia.
La ricerca sugli scimpanzé negli anni ’60 dimostrò definitivamente che la malattia di Creutzfeld-Jakob — una malattia cerebrale fatale e implacabile che sembrava essere ereditaria — poteva anche essere trasmessa dando agli scimpanzé tessuto cerebrale da animali affetti. Al microscopio, i tessuti cerebrali colpiti da kuru, scrapie o CJD apparivano tutti notevolmente simili, mostrando una caratteristica apparenza “spongiforme”. In altre parole, il tessuto cerebrale diventava pieno di buchi, come una spugna.
Eppure c’era un enigma: la CJD sembrava essere trasmessa nelle famiglie. Quindi, come potevano virus o batteri essere sia ereditari che infettivi?
Prusiner stava inizialmente studiando la CJD ma cambiò il suo focus sulla scrapie quando esaminò i dati di un team guidato da Tikvah Alper, una radiobiologa. Alper aveva scoperto che la scrapie poteva ancora essere trasmessa quando il tessuto infetto veniva irradiato con luce ultravioletta, che danneggia il DNA.

Il dottor Stanley Prusiner scoprì l’esistenza dei prioni. (Crediti immagine: Christopher Michel, CC BY 4.0 via Wikimedia Commons)
Quindi Prusiner iniziò a studiare la scrapie nei milza e nei cervelli di topi. Ma passò rapidamente ai criceti perché sviluppavano sintomi della malattia entro 70 giorni, invece di uno o due anni per i topi. Poi lavorò sistematicamente per isolare e identificare la natura chimica dell'”agente infettivo” che guidava la malattia.
Alla fine, individuò una proteina come colpevole.
“Sei linee di evidenza separate e distinte dimostrano che l’agente scrapie contiene una proteina necessaria per l’infettività”, scrisse Prusiner nello studio seminale del 1982. Tutte queste dimostrarono che la degradazione della struttura proteica interrompeva la trasmissione della scrapie. Continuò a dimostrare che non c’erano prove di acidi nucleici, come il DNA o i suoi cugini, nei campioni. Propose il nome “prione” per descrivere la proteina infettiva, che suggerì potesse “codificare per la propria biosintesi”, aggiungendo che “questa ipotesi contraddice il ‘dogma centrale’ della biologia molecolare”.
La proposta di Prusiner non fu ampiamente accettata all’inizio. Ma nei 15 anni successivi, gli scienziati chiarirono la struttura proteica dei prioni e dimostrarono che potevano assumere molteplici conformazioni, anche quando codificati dalla stessa sequenza di DNA. I ricercatori dimostrarono anche come la forma del prione resistesse alla degradazione e che poteva “convertire” le versioni sane della proteina nella forma patologica.
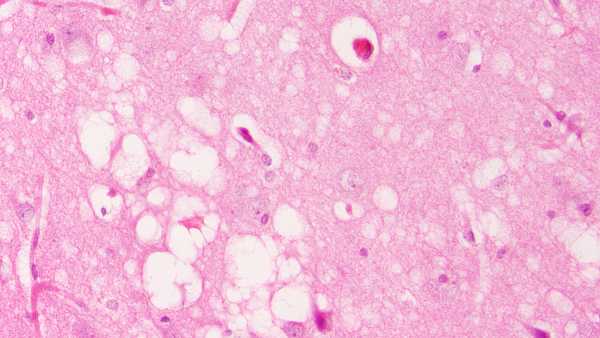
Un’immagine microscopica di tessuto cerebrale umano. I fori nel cervello (macchie bianche) sono considerati il “marchio di fabbrica” delle malattie da prioni. (Crediti immagine: UCSF via Getty Images)
Lavori successivi sui casi familiari di CJD hanno mostrato che certi geni potevano anche predisporre le persone alla malattia e che il danno al DNA determinava quanto tempo impiegava la malattia ad incubare.
Prusiner vinse il Premio Nobel per la fisiologia o la medicina nel 1997 per il suo lavoro sui prioni.
L’ipotesi di Prusiner fu convalidata quando l’epidemia di mucca pazza colpì il Regno Unito nei primi anni 2000. Gli scienziati avrebbero infine determinato che le persone venivano infettate dopo aver mangiato carne di mucche che erano state nutrite con tessuto cerebrale di mucche malate di encefalopatia spongiforme bovina (BSE). Dopo aver consumato carne di mucche con BSE, gli esseri umani sviluppano una versione della CJD nota come “variante CJD”.
ARGOMENTI
