La Dottoressa Swee Lay Thein e il Dottor Stuart Orkin hanno vinto il Breakthrough Prize in Life Sciences da 3 milioni di dollari per il loro lavoro verso una cura funzionale per le devastanti malattie del sangue, la falcemia e la beta-talassemia.
 Iscriviti alla nostra newsletter</p>
<p id=) Due scienziati il cui lavoro ha inaugurato la prima terapia approvata che utilizza lo strumento di editing genetico CRISPR hanno vinto il Breakthrough Prize in Life Sciences da 3 milioni di dollari.
Due scienziati il cui lavoro ha inaugurato la prima terapia approvata che utilizza lo strumento di editing genetico CRISPR hanno vinto il Breakthrough Prize in Life Sciences da 3 milioni di dollari.
I premiati — la Dottoressa Swee Lay Thein, del National Heart, Lung and Blood Institute (NHLBI), e il Dottor Stuart H. Orkin, della Harvard University — si sono divisi il premio per la ricerca di base che ha portato allo sviluppo di una terapia genica che tratta i disturbi del sangue, la falcemia e la beta-talassemia.
Il Breakthrough Prize in Life Sciences viene assegnato dal 2013 per riconoscere i successi nelle scienze della vita.
Devastanti malattie del sangue
La falcemia colpisce circa 7-8 milioni di persone a livello globale, prevalentemente in Africa. Nei soggetti affetti da questo disturbo, i globuli rossi assumono una caratteristica forma a mezzaluna perché l’emoglobina, la molecola trasportatrice di ossigeno all’interno delle cellule, forma fibrille rigide e lunghe che deformano le cellule. Queste cellule falciformi si attaccano l’una all’altra, scatenando coaguli di sangue, e inoltre scoppiano e muoiono facilmente, causando bassi livelli di globuli rossi.
I pazienti spesso affrontano episodi di dolore lancinante, noti come “crisi”, quando i globuli rossi bloccano i vasi sanguigni. Questi blocchi possono danneggiare organi come polmoni, fegato e milza. I blocchi nei polmoni possono anche scatenare la “sindrome toracica acuta”, che riduce i livelli di ossigeno ed è la principale causa di morte nei pazienti affetti da falcemia.
Nella beta-talassemia, il corpo non produce — o produce in quantità ridotte — una parte della molecola di emoglobina, il che significa che le persone con forme gravi della malattia devono sottoporsi a trasfusioni di sangue a vita. Casgevy è approvato per il trattamento di questa forma grave della malattia.
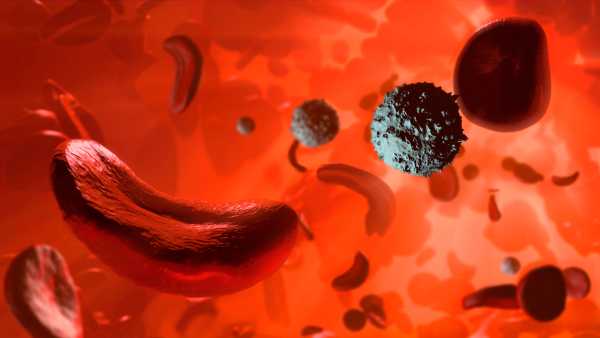
Le cellule falciformi assumono la loro forma caratteristica perché la molecola di emoglobina forma fibrille lunghe e rigide che deformano la forma dei globuli rossi. (Crediti immagine: MARK GARLICK/SCIENCE PHOTO LIBRARY via Getty Images)
La Thein, ricercatrice senior presso l’NHLBI, ha iniziato il suo lavoro negli anni ’80 cercando di capire perché alcune persone con questi disturbi avessero forme molto più lievi delle malattie rispetto ad altre.
La questione era emersa decenni prima, quando la Dottoressa Janet Watson, una pediatra di New York, aveva dimostrato che i neonati che in seguito sviluppavano la falcemia non presentavano sintomi e avevano globuli rossi che non si falcizzavano.
Una volta diventati bambini, emergevano i sintomi della malattia.
Lavori successivi hanno dimostrato che le persone producono diversi tipi di emoglobina in diverse fasi di sviluppo: l'”emoglobina fetale” viene prodotta nell’utero, la sua produzione viene interrotta man mano che i neonati maturano e subentra l'”emoglobina adulta”.

Swee Lay Thein è un’ematologa e medico malese presso il National Institute of Health (NIH) e co-vincitrice del Breakthrough Prize 2026. (Crediti immagine: Jackie Lee)
“Ho iniziato a raccogliere famiglie — pazienti — con talassemia lieve, per cercare almeno di svelare la genetica alla base,” ha detto la Thein a Live Science. “Sembrava ovvio che avessero una capacità innata, o naturale, di continuare a produrre emoglobina fetale.”
Ha analizzato i geni di diverse famiglie che avevano una storia di malattia, inclusa una famiglia di origine indiana che comprendeva più di 200 membri, si estendeva su sette generazioni e viveva in più continenti.
Repressione del repressore
Una svolta cruciale è arrivata da uno studio su coppie di gemelli identici e fraterni che producevano livelli molto alti o molto bassi di emoglobina fetale. Questo ha permesso alla Thein e ai suoi colleghi di identificare varianti genetiche che influenzavano la produzione di emoglobina fetale. Si sono concentrati su una regione di un gene sul cromosoma 11 chiamata BCL11A.
Il team della Thein ha scoperto che il gene spegne la produzione di emoglobina fetale man mano che i neonati crescono. “È un repressore,” ha detto la Thein. Ma quando le persone portavano certe versioni di BCL11A, il repressore non reprimeva e la produzione di emoglobina fetale continuava a livelli elevati per tutta la vita.
Da lì, non è stato un salto drammatico concludere che reprimere il repressore potesse essere una buona strategia per trattare persone con forme gravi di falcemia o beta-talassemia. La ricerca di Orkin si è rivelata fondamentale per fare questo salto.
Orkin — che è un ematologo e oncologo pediatrico presso il Boston Children’s Hospital, il Dana-Farber Cancer Institute, la Harvard Medical School e l’Howard Hughes Medical Institute — ha dimostrato come il repressore mediase il passaggio all’emoglobina adulta, e che l’editing genetico potesse colpire quella regione.
La società biotecnologica Vertex ha quindi utilizzato lo strumento di editing genetico “taglia e incolla” CRISPR per rimuovere la regione repressore di BCL11A.
Questo lavoro ha infine portato allo sviluppo di Casgevy. La somministrazione della terapia prevede l’estrazione delle cellule staminali del midollo osseo di una persona, l’editing del repressore BCL11A utilizzando CRISPR, e quindi la reinfusione delle cellule staminali del midollo osseo modificate geneticamente nel paziente. Le cellule modificate iniziano a produrre globuli rossi con alti livelli di emoglobina fetale.

Stuart Orkin ha dimostrato che BCL11A poteva essere un bersaglio valido per una terapia genica per la falcemia e la beta-talassemia. (Crediti immagine: Scott Eisen/Howard Hughes Medical Institute)
È la prima “cura funzionale” per la falcemia, e ha trasformato la vita di pochi che l’hanno ricevuta. Ma non è una cura disponibile per tutti con la malattia, e ci sono alcuni svantaggi, ha detto la Thein. Il processo di trattamento stesso può richiedere fino a un anno, costa diversi milioni di dollari e richiede una chemioterapia aggressiva per fare spazio nel midollo osseo affinché le cellule staminali modificate geneticamente attecchiscano.
“Fisicamente, è molto estenuante per il paziente,” ha detto la Thein.
Inoltre, la falcemia e la beta-talassemia colpiscono prevalentemente persone in Africa, Asia e nel Mediterraneo, dove le risorse e le strutture necessarie per tali trattamenti potrebbero non essere disponibili. Di conseguenza, gli scienziati che lavorano alla terapia genica stanno passando a un approccio “in vivo”, che implica “l’iniezione effettiva del macchinario di editing genetico nel paziente,” ha detto la Thein. Questo eliminerebbe la necessità di estrarre, modificare e reinfondere le cellule staminali del midollo osseo.
In definitiva, la necessità di farmaci più numerosi — inclusi pillole, iniezioni o infusioni più economiche e facili da somministrare — è ancora pressante, ha detto la Thein.
La Thein ha studiato un farmaco chiamato Mitavipat. Il farmaco, attualmente approvato per il trattamento della malattia del sangue deficit di piruvato chinasi e della beta-talassemia, sembra funzionare migliorando la salute metabolica generale dei globuli rossi, ha detto la Thein.
Alcuni pazienti che assumono questo farmaco sono “in questo trattamento con me da sei anni, e ha davvero fatto una grande differenza,” ha detto, ma sono necessari ulteriori test per approvarne l’uso nelle persone con falcemia.
ARGOMENTI
