C’est une blague récurrente dans la communauté du diabète de type 1 qu’un remède est “à seulement cinq ans” et ce, depuis au moins 50 ans. Cependant, de nouveaux essais sur les cellules souches et des médicaments immunitaires suggèrent que nous nous rapprochons plus que jamais d’un remède fonctionnel pour la maladie.
Il y a une blague récurrente dans la communauté du diabète de type 1 selon laquelle un remède est “à seulement cinq ans”. Mais il y a peut-être un fond de vérité dans cette affirmation maintenant. (Crédit photo : photomontage de Marilyn Perkins ; ressources de Tatiana Cheremukhina et STEVE GSCHMEISSNER/SCIENCE PHOTO LIBRARY via Getty Images) Abonnez-vous à notre newsletter
Mon premier indice que quelque chose n’allait pas était l’odeur de barbe à papa.
C’était le 15 mars 2016, et je changeais les draps de mon tout-petit parce qu’il avait traversé sa couche. Le lit était mouillé, mais il ne sentait pas l’urine. D’autres détails que j’avais négligés me sont venus à l’esprit, et j’ai commencé à m’inquiéter.
S’il vit jusqu’à un âge avancé, il aura changé le capteur qui mesure son taux de sucre dans le sang et le “site” — le tube qui délivre l’insuline — des dizaines de milliers de fois, aura passé plus d’un demi-million d’heures avec un taux de sucre dans le sang élevé ou bas, et aura accumulé des millions de dollars de soins médicaux. Se libérer de ces montagnes russes de la glycémie changerait radicalement son avenir.

Science Spotlight examine les sciences émergentes en profondeur et vous offre, à vous, nos lecteurs, la perspective dont vous avez besoin sur ces avancées. Nos histoires mettent en lumière les tendances dans différents domaines, la façon dont la recherche nouvelle change les anciennes idées, et comment l’image du monde dans lequel nous vivons est transformée grâce à la science.
“Je pourrais mieux dormir. Et je n’aurais pas à changer de site ou de capteur, ni à faire d’injections”, a dit mon fils. “Ce serait une meilleure vie.”
Il y a une blague récurrente dans la communauté du diabète de type 1 selon laquelle un remède est “à seulement cinq ans” — et ce, depuis au moins 50 ans.
Mais il y a peut-être un fond de vérité maintenant.
Les premiers traitements visant à remplacer les cellules bêta détruites sont en phase avancée d’essais qui devraient se conclure dans les prochaines années. Et les scientifiques développent des moyens innovants pour maintenir ces cellules transplantées en vie sans effets secondaires nocifs.
De nombreux obstacles subsistent avant que de tels traitements puissent être largement utilisés chez les enfants atteints de la maladie. Mais une image d’un monde post-diabète de type 1 (DT1) émerge. Dans un avenir pas si lointain, ceux qui ont une glycémie dangereusement erratique ou qui doivent déjà supprimer leur système immunitaire pour d’autres raisons pourraient être libérés de la maladie grâce à des greffes de cellules souches. Et après cela, des adultes et des enfants autrement en bonne santé pourraient recevoir des greffes de cellules souches.
“Les thérapies de remplacement cellulaire sont notre programme phare car nous pensons qu’il est imminent de fournir un remède fonctionnel aux personnes atteintes de diabète de type 1”, c’est-à-dire que les symptômes de la maladie sont éliminés, a déclaré le Dr Sanjoy Dutta, directeur scientifique de Breakthrough T1D, une organisation à but non lucratif qui soutient la recherche et la défense des droits pour prévenir, traiter et guérir la maladie.

Mon fils avait moins de 2 ans lorsqu’il a été diagnostiqué diabétique. Peu après le diagnostic, il s’est vu prescrire un moniteur de glucose continu (CGM), qu’il porte en permanence. Sur cette photo, vous pouvez voir le contour du CGM sous sa manche. (Crédit photo : Tia Ghose)De la condamnation à mort à la maladie chronique
Le symptôme le plus frappant de mon fils — l’odeur sucrée de son urine — était un signe typique de la maladie. “Diabetes mellitus” (le nom complet de la maladie) signifie “siphon sucré” en grec, et ses symptômes ont été décrits pour la première fois il y a 3 500 ans dans l’Égypte ancienne.
Nous savons maintenant que le diabète de type 1 survient lorsque le système immunitaire détruit par erreur les cellules bêta productrices d’insuline dans le pancréas, qui sont regroupées dans des cellules appelées îlots.
En conséquence, le corps ne peut pas transporter le glucose dans les tissus. Au lieu de cela, le glucose s’accumule dans le sang, et les reins travaillent à plein régime pour tenter de l’éliminer. Pendant ce temps, les tissus musculaires et adipeux meurent de faim. Sans glucose comme source d’énergie, le corps décompose les graisses pour obtenir de l’énergie et les transforme en composés appelés cétones. Ce processus gourmand en eau déshydrate davantage le corps, et ces cétones s’accumulent dans le sang, le rendant acide.
Une personne atteinte de diabète de type 1 non traité aura une faim et une soif insatiables. À mesure qu’elle mange et boit, et urine et urine, son corps se dévorera lentement à mesure que ses graisses et ses muscles fondront. Sans traitement, une personne atteinte de diabète de type 1 tombera inévitablement dans le coma et mourra.

Grâce aux moniteurs de glucose continus, les personnes atteintes de diabète peuvent obtenir des lectures de leur glycémie jusqu’à chaque minute. (Crédit photo : Svetlana Repnitskaya via Getty Images)
La solution à ce problème est l’insuline. En 1921, Frederick Banting et Charles Best ont isolé l’insuline des cellules des îlots pancréatiques chez des chiens et ont finalement mis au point un moyen de produire de l’insuline à partir du pancréas d’une vache.
La science avait transformé le diabète de type 1 d’une condamnation à mort en une maladie chronique — un accomplissement qui a valu à Banting le prix Nobel de médecine en 1923.
Nous avons parcouru un long chemin depuis. Les gens vivent maintenant couramment des décennies après leur diagnostic. Les scientifiques ont créé une insuline à action plus rapide, conçu des pompes à insuline qui automatisent la délivrance du médicament, et développé des moniteurs de glucose continus qui révèlent les niveaux de sucre dans le sang jusqu’à chaque minute. Ces innovations améliorent les niveaux moyens de sucre dans le sang et réduisent les complications.
Même il y a cinq ans, je n’aurais pas prédit que nous serions aussi avancés que nous le sommes.
Lori Sussel, directrice de la recherche de base et translationnelle au Barbara Davis Center for Diabetes de l’University of Colorado Anschutz Medical Campus
Cependant, aucune de ces avancées n’a fondamentalement changé la nature implacable de la maladie. L’insuline injectée n’agit pas aussi vite que la version produite par le corps. Et comme des dizaines de facteurs — y compris l’alimentation, l’exercice, le stress, la maladie et la puberté — peuvent affecter la quantité d’insuline dont le corps a besoin, les patients sont toujours à risque de sous- ou sur-doser l’insuline.
“C’est une maladie qui nécessite une gestion surhumaine 24h/24 et 7j/7”, a déclaré Dutta à Live Science.
Les personnes qui s’injectent de l’insuline font généralement face à des heures de glycémie élevée et basse chaque jour. Des décennies d’hyperglycémie peuvent détruire les reins, endommager les nerfs et provoquer la cécité et des crises cardiaques. Une hypoglycémie critique peut tuer en quelques heures, car le cerveau est privé d’énergie.
Malgré les progrès médicaux, le diabète de type 1 réduit en moyenne l’espérance de vie de plus d’une décennie.
Remplacement des cellules perdues
La réduction de la durée et de la qualité de vie a poussé les scientifiques à continuer à chercher un remède contre le diabète. La simple gestion de la maladie n’est pas suffisante.
Depuis les années 1990, plus de 1 000 personnes dans le monde ont reçu des greffes de cellules d’îlots provenant de cadavres ; aux États-Unis, cela reste une procédure expérimentale, donc elle n’est réalisée que dans le cadre d’essais cliniques. Certains des receveurs de cellules d’îlots ont été guéris de la maladie — du moins temporairement.
Mais les pancréas de donneurs dont proviennent les cellules d’îlots sont très rares. Et les cellules peuvent être endommagées, avant ou pendant la récolte, donc leur qualité est souvent médiocre. Par conséquent, les greffes de cellules d’îlots de cadavres ne sont pas très efficaces ; cinq ans après la transplantation, seulement 1 personne sur 10 qui en reçoit n’a pas besoin de s’injecter d’insuline.
Un autre défi est que les receveurs doivent prendre des médicaments immunosuppresseurs à vie. Par conséquent, les greffes de cadavres sont principalement proposées aux personnes qui ont déjà besoin d’un autre type de greffe, comme une greffe de rein.
Pour que les greffes d’îlots représentent un remède viable, elles doivent être faciles à produire en masse avec une qualité constante et élevée, et les scientifiques doivent empêcher le système immunitaire de détruire les cellules d’îlots.
Nous nous rapprochons très près de ce premier objectif : produire des cellules bêta de haute qualité à partir de rien.
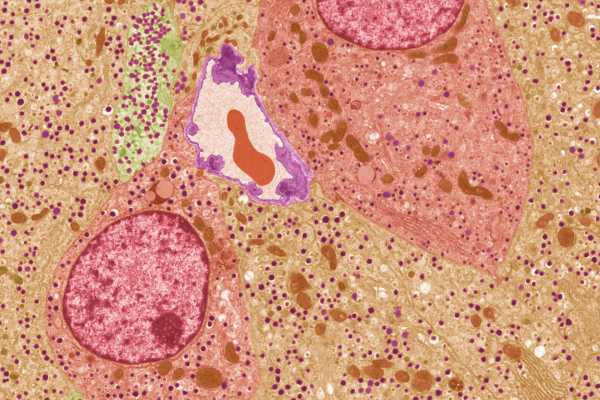
Des cellules des îlots pancréatiques au microscope. Les îlots sont des amas de cellules qui produisent diverses hormones, dont l’hormone abaissant la glycémie, l’insuline. (Crédit photo : STEVE GSCHMEISSNER/SCIENCE PHOTO LIBRARY via Getty Images)De la cellule embryonnaire à la cellule bêta
Au cours des dernières années, les scientifiques ont fait d’incroyables progrès dans le décryptage de la symphonie chimique qui dirige les cellules souches embryonnaires pluripotentes — des cellules qui peuvent devenir n’importe quel type de cellule du corps — pour se métamorphoser en îlots.
“Même il y a cinq ans, je n’aurais pas prédit que nous étions aussi avancés que nous le sommes”, a déclaré Lori Sussel, directrice de la recherche de base et translationnelle au Barbara Davis Center for Diabetes de l’University of Colorado Anschutz Medical Campus, qui mène des recherches de base sur les îlots en utilisant des modèles de cellules souches humaines et murines.
Certains traitements basés sur cette recherche sont déjà en phase de développement avancé. Par exemple, Vertex Pharmaceuticals, une société de biotechnologie basée à Boston, a rapporté en 2025 dans le The New England Journal of Medicine (NEJM) que 10 des 12 patients ayant reçu le produit de la société dérivé de cellules souches embryonnaires, appelé VX-880, n’ont pas besoin de prendre d’insuline un an après leur greffe. Et tous produisent une certaine quantité d’insuline, a déclaré Felicia Pagliuca, vice-présidente principale de la recherche sur les thérapies cellulaires et génétiques chez Vertex, à Live Science.
(Les deux patients qui sont restés dépendants de l’insuline ont pris des stéroïdes pendant le traitement, contre les instructions de l’étude. Les stéroïdes augmentent la glycémie, ce qui peut endommager les cellules bêta, ont écrit les auteurs de l’étude NEJM.)
L’essai a débuté avec 14 participants, mais deux personnes sont décédées pendant celui-ci. Cependant, les auteurs de l’étude, et vraisemblablement les conseils de surveillance de la sécurité pour l’essai, ont conclu que ces décès n’étaient pas liés au traitement. Néanmoins, comme pour tout traitement potentiel, plus de données sont nécessaires pour voir si d’autres problèmes surgissent chez les patients subissant ces greffes.
L’immunosuppression est pire que de devoir prendre de l’insuline tous les jours.
Lori Sussel, directrice de la recherche de base et translationnelle au Barbara Davis Center for Diabetes de l’University of Colorado Anschutz Medical Campus
L’entreprise fait précisément cela, en testant le VX-880 dans un essai plus large qui inclura 50 patients atteints d’hypoglycémie non reconnue, c’est-à-dire qu’ils ne ressentent pas physiquement quand leur glycémie devient dangereusement basse. Ces patients présentent un risque de mortalité de base plus élevé, a déclaré Sussel. L’essai nécessitera un an de données avant de pouvoir être soumis à la Food and Drug Administration, a dit Pagliuca. Mais si ces résultats sont positifs, cela signifierait qu’une source évolutive de cellules souches fiables pourrait être disponible pour certaines personnes atteintes de diabète de type 1.
Vertex n’est pas la seule équipe à travailler sur la reprogrammation des cellules pour qu’elles deviennent des îlots. Des chercheurs en Chine ont reprogrammé les propres cellules adipeuses d’une femme pour en faire des cellules bêta. Un avantage de cette approche est que ces cellules ne sont pas immédiatement reconnues comme étrangères, car elles proviennent du corps du patient. Un inconvénient, cependant, est que la création d’un traitement unique pour chaque individu est susceptible d’être prohibitivement coûteuse en tant que remède à grande échelle, a déclaré Sussel.
Cape d’invisibilité immunitaire
La création des cellules souches n’est que la première étape. Une fois dans le corps, elles doivent survivre. Cela a historiquement nécessité des médicaments immunosuppresseurs puissants, tout comme les autres greffes.
Les médicaments immunosuppresseurs — tels que le tacrolimus et le sirolimus — rendent les personnes sensibles aux infections et peuvent endommager les reins, et peuvent augmenter le risque de cancer. Le tacrolimus est également toxique pour les cellules d’îlots transplantées elles-mêmes, a déclaré le Dr Piotr Witkowski, directeur du programme de transplantation de pancréas et d’îlots pancréatiques à l’UChicago Medicine.
Mais le jeune atteint de diabète de type 1 a des décennies de vie relativement saine devant lui, donc mettre son cœur et ses reins en danger avec des médicaments immunosuppresseurs présente un risque plus élevé que le bénéfice.
“L’immunosuppression est pire que de devoir prendre de l’insuline tous les jours”, a dit Sussel à Live Science. En pensant à cela pour mon propre fils, je ne peux qu’être d’accord ; le diabète est un énorme inconvénient, mais prendre le risque d’infections mortelles ou de taux de cancer plus élevés à long terme pour éliminer cet inconvénient ne semble pas en valoir la peine.
Les scientifiques explorent plusieurs façons de résoudre le problème de l’attaque immunitaire.

Alors que de nombreux enfants ont maintenant leur taux de sucre dans le sang surveillé par un CGM attaché au corps, beaucoup de gens utilisent encore une technologie plus ancienne pour vérifier ponctuellement leur glycémie. Cela implique de faire une piqûre au doigt pour tester leur sang à l’aide d’un glucomètre. (Crédit photo : Svetlana Repnitskaya via Getty Images)
L’une d’elles consiste à rendre les cellules bêta transplantées “invisibles” au système immunitaire. Pour ce faire, une entreprise s’inspire de la grossesse. Pendant la grossesse, 50% des gènes — et donc des protéines — du fœtus proviennent du père, a déclaré le Dr Sonja Schrepfer, fondatrice scientifique de Sana Biotechnology (Hypoimmune Platform) basée à Seattle et scientifique chercheuse au Cedars Sinai Medical Center à Los Angeles.
Schrepfer et son équipe ont donc étudié quelles molécules aident à protéger le fœtus des attaques immunitaires pour maintenir la grossesse.
Elles en ont identifié quelques-unes. Deux molécules agissent comme des empreintes digitales uniques présentes à l’extérieur de chaque cellule du corps. Lorsque le système immunitaire détecte une empreinte étrangère, il détruit les cellules qui la portent. Pendant la grossesse, le fœtus réduit le nombre de ces empreintes digitales produites, en particulier dans le placenta, a déclaré Schrepfer. Donc, pour protéger les cellules d’îlots transplantées du système immunitaire, “nous devons nous débarrasser de cette empreinte digitale”, a dit Schrepfer à Live Science.
Mais ce n’est que la première étape pour prévenir le rejet. Certaines cellules immunitaires, appelées cellules tueuses naturelles et macrophages, patrouillent constamment le corps et tuent automatiquement les cellules sans empreinte digitale, a-t-elle dit.
La mise à l’échelle sera très coûteuse, et donc je pense qu’en ce moment, c’est probablement l’une des étapes limitantes, c’est le coût.
Lori Sussel, directrice de la recherche de base et translationnelle au Barbara Davis Center for Diabetes de l’University of Colorado Anschutz Medical Campus
Cependant, la recherche de Schrepfer a montré que les cellules produisent naturellement une molécule spéciale, à de faibles niveaux, qui crie essentiellement “Ne me tuez pas”. Lorsque les cellules surexpriment cette molécule, les macrophages et les cellules tueuses naturelles s’approchent des cellules transplantées mais s’en éloignent ensuite, laissant les cellules tranquilles, a dit Schrepfer.
Sana Biotechnology a donc utilisé l’outil d’édition génétique CRISPR, ainsi qu’un virus inoffensif, pour modifier génétiquement des cellules bêta prélevées sur un cadavre afin qu’elles n’aient plus les empreintes digitales cellulaires et qu’elles surexpriment la molécule “ne me tuez pas”. Ces cellules “hypoimmunitaires” sont, en théorie, tolérées par le système immunitaire.
En août 2025, Sana a rapporté avoir traité le premier patient avec ces cellules plus tôt cette année, et en mars 2026, elle a annoncé que les cellules échappaient toujours au système immunitaire et produisaient de l’insuline. Bien que des essais de sécurité et d’efficacité plus importants soient encore loin, les nouveaux résultats suscitent l’espoir que cette approche conduira à des cellules bêta dérivées de cellules souches qui ne nécessitent pas d’immunosuppression.
Vertex Pharmaceuticals étudie également des greffes de cellules souches génétiquement modifiées qui peuvent échapper à la détection immunitaire, mais l’entreprise ne les a pas encore testées chez l’homme, a indiqué Pagliuca.
Médicaments plus doux
D’autres moyens de prévenir le rejet de greffe sont en cours de développement. Contrairement aux cellules d’îlots génétiquement modifiées, ces méthodes reposent sur une voie d’approbation des médicaments plus établie.
L’un d’eux est un médicament appelé tegoprubart, qui a été initialement développé pour prévenir le rejet de greffe rénale. (Il est également à l’essai pour retarder la progression de la SLA.)
Lorsque les cellules immunitaires reconnaissent pour la première fois une protéine étrangère, elles ont besoin d’un second signal pour mobiliser le reste du système immunitaire à attaquer, a expliqué Witkowski à Live Science. Le tegoprubart supprime ce second “signal d’attaque” en inactivant une molécule appelée ligand CD40, a-t-il dit.
Dans une étude impliquant 12 patients, Witkowski et ses collègues ont transplanté des cellules d’îlots de cadavres et ont donné aux participants du tegoprubart au lieu du médicament standard, le tacrolimus. Le tegoprubart a conduit à une meilleure survie des cellules bêta qu’avec le tacrolimus.
En mars, Witkowski a présenté des résultats lors d’une conférence sur le diabète montrant que les 10 patients qui ont reçu des greffes plus de quatre semaines auparavant sont jusqu’à présent sans insuline et qu’aucun des participants n’a présenté d’effets secondaires graves ou de rejet.
Plus tard cette année, l’équipe prévoit également de lancer un essai de 10 personnes avec Breakthrough T1D pour tester le tegoprubart chez les personnes souffrant de dysfonction rénale et de DT1 — un groupe qui a historiquement été empêché de subir ces greffes, a dit Witkowski.
De plus, le tegoprubart n’est qu’un des plusieurs protocoles immunosuppresseurs plus doux qui sont actuellement étudiés, a déclaré Dutta. D’autres incluent l’anti-thymocyte globuline et le teplizumab, un médicament qui a été démontré pour prévenir la progression du diabète de type 1 à un stade précoce, a-t-il ajouté.
Je détesterais dire que nous sommes à cinq ans. Ce que je dirais, c’est qu’un remède est à l’horizon.
Lori Sussel, directrice de la recherche de base et translationnelle au Barbara Davis Center for Diabetes de l’University of Colorado Anschutz Medical Campus

Pour mon fils, savoir que les chercheurs travaillent sur un remède contre le diabète de type 1 lui donne de l’espoir. (Crédit photo : Tia Ghose)Espoir à l’horizon
La recherche sur le diabète de type 1 est jalonnée de dizaines de remèdes autrefois prometteurs qui se sont finalement avérés décevants, il est donc judicieux d’être prudent quant à ces nouvelles approches.
En effet, il reste encore quelques problèmes à résoudre. Par exemple, lorsque les cellules souches embryonnaires sont converties en cellules bêta, la plupart des cellules résultantes produisent de l’insuline, mais certaines produisent également d’autres hormones, comme le glucagon, qui augmente la glycémie, et la somatostatine, qui inhibe l’hormone de croissance, a dit Sussel. De plus, le processus de fabrication de ces cellules est laborieux et prend du temps.
“La mise à l’échelle sera très coûteuse, et donc je pense qu’en ce moment, c’est probablement l’une des étapes limitantes, c’est le coût”, a dit Sussel.
Et, bien sûr, des études à plus long terme devront déterminer la durée des greffes de cellules souches et si elles doivent être administrées périodiquement. Il pourrait également y avoir des effets secondaires qui prennent des années ou des décennies à apparaître. En tant que parent, je devrais être convaincu que les décès observés dans l’essai Vertex étaient complètement sans rapport avec le traitement avant de m’engager.
Tous ceux à qui j’ai parlé se méfiaient de fixer un calendrier pour un avenir post-diabète.
“Je détesterais dire que nous sommes à cinq ans”, a dit Sussel. “Ce que je dirais, c’est qu’un remède est à l’horizon.”
Mais il y avait une excitation palpable parmi les chercheurs à qui j’ai parlé, tous disant que les percées arrivaient à un rythme rapide.
Un monde où personne n’a le diabète de type 1 est encore loin. Mais petit à petit, un remède fonctionnel arrive pour de plus en plus de personnes.
“Idéalement, tout le monde en bénéficiera un jour, mais nous allons commencer petit puis passer au grand”, a dit Dutta.
Mon fils réalise qu’il ne verra probablement pas de remède avant un certain temps. Mais savoir que quelque chose arrive lui donne de l’espoir. Et ce serait d’autant plus déchirant si ces traitements ne fonctionnaient pas.
“Quand je m’imagine adulte, je ne me vois pas avec le diabète”, a-t-il dit.
“Je serai très déçu si ces traitements ne fonctionnent pas.”
SUJETS
